Глиобластома относится к числу самых агрессивных и трудно поддающихся лечению опухолей головного мозга, характеризующихся высокой инвазивностью и быстрой регенерацией после хирургического вмешательства. Одной из главных проблем терапии является сложность точного визуального определения границ новообразования во время операции, что часто приводит к сохранению микроскопических скоплений злокачественных клеток и, как следствие, рецидивам. В связи с этим, развитие современных методов визуализации в режиме реального времени приобретает первостепенное значение для усовершенствования хирургических методик и улучшения прогноза пациентов. Современная медицина давно использует различные оптические и ядерно-медицинские препараты для меток опухолевых клеток, однако они обладают рядом ограничений. Радиоактивные препараты, хотя и позволяют выявлять активные метаболические процессы, сопровождаются воздействием ионизирующего излучения, высокой стоимостью и технической сложностью проведения исследований.
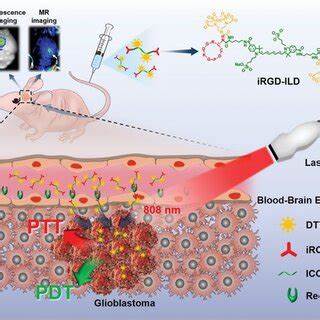
Традиционные флуоресцентные красители, такие как 5-аминолевулиновая кислота (5-ALA), широко применяются в глиохирургии, однако имеют ограниченную глубину проникновения света и недостаточную специфичность, а также фотоблеачинг и фоточувствительность, что негативно сказывается на точности и удобстве их использования во время операции. В этом контексте большой интерес представляет новейшая разработка — молекулярный жирнокислотный зонд FA-ICG, сочетающий в себе длинноцепочечную насыщенную жирную кислоту (пальмитиновую кислоту) и близкоинфракрасный краситель индотцианиновый зеленый (ICG). Такое соединение позволяет специфически нацеливаться на процессы метаболизма жирных кислот, активно эксплуатируемые злокачественными клетками, включая глиобластому, и одновременно обеспечивает глубокое проникновение и высокое отношение сигнал/шум за счет использования ближней инфракрасной области спектра. Принцип действия FA-ICG основан на модификации естественного пути абсорбции и транспорта длинноцепочечных жирных кислот в клетках через соответствующие транспортные белки, такие как FATP (Fatty Acid Transport Proteins). Поскольку многие опухолевые клетки глиобластомы обладают усиленным захватом и метаболизмом жирных кислот, молекулярный зонд эффективно накапливается в опухолевых тканях.
Это обеспечивает высокую контрастность изображения и позволяет отличить опухоль от окружающей здоровой ткани с большей точностью, нежели традиционные методы. В ряде исследований было продемонстрировано, что FA-ICG обладает стабильным спектром поглощения с пиком около 780 нм и излучения — около 820 нм, что оптимально для внутритканевого распространения света и минимального поглощения биологическими хромофорами. Такая особенность сокращает эффект аутосвечения тканей, увеличивает сигнал и облегчает выделение опухолевых структур. Кроме того, использование FDA-одобренного красителя ICG повышает безопасность и перспективы клинической трансляции данного подхода. Эксперименты in vitro на клеточных культурах 3T3-L1 и различных раковых линиях показали, что FA-ICG действительно имитирует естественную передачу жирных кислот, проявляя дозозависимый и селективный захват именно клетками с активным жировым обменом.
В частности, глиобластомные клетки линии U87-MG демонстрируют высокий уровень поглощения зонда, а конкурирующее введение естественной олеиновой кислоты значительно уменьшает этот захват, подтверждая специфичность взаимодействия. Такой экспресс-тест важен для понимания механизма действия и гарантирует, что сигнал флуорофора обусловлен именно включением в метаболизм жирных кислот, а не неспецифическим связыванием. Дальнейшие данные in vivo, полученные на ортотопических модельных животных, моделирующих глиобластому человека, подтвердили высокую способность FA-ICG к накоплению в опухолевой ткани мозга при сравнении с неизмененным ICG. Измерения с помощью систем IVIS Spectrum и FMT-(CT) позволили получать неинвазивные трехмерные изображения с хорошим цветовым контрастом и высоким коэффициентом опухоль/нормальная ткань. Максимальное соотношение сигнал/фон достигалось через 12-24 часа после внутривенного введения, что отлично вписывается в операционные протоколы.
Экскреция зонда, главным образом печенью и почками, не мешает наблюдению опухоли и не вызывает токсичности. Особый акцент сделан на возможностях применения FA-ICG для хирургического вмешательства с визуальным контролем. В экспериментальных операциях мышам с имплантированными глиобластомами удалось четко визуализировать опухолевую массу в мозге с помощью стандартной клинической камеры NIR (QUEST Spectrum® 2). Использование зонда позволило лучше определить границы новообразования, чем контроль с ICG, и обеспечило более точное иссечение, что критично для сохранения здоровой мозговой структуры и уменьшения неврологических осложнений. Важным этапом была апробация технологии на компаньонных собаках с мастоцитомой, опухолью, которая по патологии во многом схожа с человеческой.
Здесь тоже удалось успешно применить FA-ICG для интраоперационного обозначения опухолевой зоны, что свидетельствует о потенциале трансляции метода в ветеринарную и, особенно, клиническую практику. Таким образом, жирнокислотный молекулярный зонд FA-ICG объединяет преимущества высокоселективного метаболического таргетирования и оптимальных оптических характеристик ближнего инфракрасного диапазона. Это обеспечивает сверхчувствительное, специфичное и глубоко проникающее изображение глиобластомы в реальном времени. Представленная технология подтверждает теоретическую и практическую возможность улучшения исходов хирургического лечения за счет повышения точности удаления опухоли и минимизации инвазивных повреждений. На текущем этапе продолжаются исследования по изучению фармакокинетики, безопасности и оптимизации формирования препарата для человека.
Открывается перспектива проведения клинических испытаний с целью подтверждения эффективности в условиях операционной. В долгосрочной перспективе такая методика способна не только повысить выживаемость и качество жизни пациентов с глиобластомой, но и найти применение в диагностике и хирургическом лечении других форм онкологической патологии с измененным липидным метаболизмом. Инновации в области оптической визуализации и молекулярных зондов, подобные FA-ICG, знаменуют собой следующий этап эволюции онкохирургии. Сливая знания о биохимии опухолевого метаболизма с передовыми визуализационными технологиями, они открывают новые горизонты для персонализированной, безопасной и максимально эффективной медицины в сфере нейроонкологии.