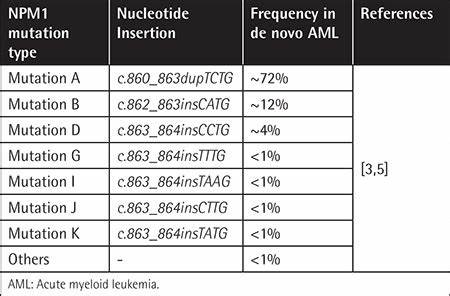
Острая миелоидная лейкемия (ОМЛ) представляет собой одну из самых агрессивных форм злокачественных заболеваний крови, требующую точной диагностики и эффективного лечения. Несмотря на значительный прогресс в области терапии, риск рецидива после первичной ремиссии остаётся высокой проблемой, что обусловливает необходимость поиска точных прогностических маркеров. Одним из перспективных индикаторов риска рецидива у пациентов с ОМЛ является мутация в гене NPM1 – нуклеофосмин, играющий ключевую роль в регуляции различных клеточных процессов, включая транспорт белков и поддержание целостности генома.Мутации в NPM1 встречаются примерно у половины пациентов с ОМЛ, относящихся к группе стандартного цитогенетического риска. Их выявление осуществляется с помощью высокочувствительных методов ПЦР, позволяющих обнаруживать минимальную остаточную болезнь (МРО) даже в периферической крови.
Наличие трансриптов мутированного NPM1 служит маркером остатков злокачественных клеток, что напрямую связано с вероятностью рецидива заболевания.Исследования, проведённые британским Национальным исследовательским институтом рака, включали анализ образцов от 346 пациентов с подтверждённой мутацией NPM1. Результаты показали, что у 15% пациентов после двух циклов химиотерапии можно было выявить мутированные трансрипты NPM1, что существенно повышало риск повторного появления болезни. Конкретно, через три года риск рецидива у этой группы составил 82%, тогда как у пациентов без таких трансриптов — около 30%. Помимо вероятности рецидива, у пациентов с положительным тестом наблюдалась значительно сниженная общая выживаемость – 24% по сравнению с 75% у пациентов с отрицательным результатом.
Этот факт подчёркивает клиническую значимость своевременного и точного мониторинга минимальной остаточной болезни у больных ОМЛ с мутацией NPM1. Ранее решение о проведении аллогенной трансплантации стволовых клеток зачастую опиралось на цитогенетический риск, и пациенты со стандартным риском не всегда направлялись на этот вид терапии из-за потенциально высокой сопутствующей смертности, особенно при наличии сопутствующих заболеваний. Однако выявление минимальной остаточной болезни по мутации NPM1 создаёт возможность более чёткого определения необходимости агрессивного лечения, что может привести к повышению числа пациентов, проходящих трансплантацию и улучшению их шансов на излечение.Помимо мутации NPM1, прогноз у пациентов с ОМЛ дополнительно может влиять наличие патологий в генах FLT3 и DNMT3A. Взаимодействие этих генетических факторов создаёт сложную картину прогноза и требует интеграции нескольких маркеров для создания более точной и индивидуализированной схемы лечения.
Современные методы молекулярной диагностики, позволяющие отслеживать мутированные трансрипты в периферической крови, делают мониторинг более удобным и менее инвазивным, что способствует частому контролю состояния пациента и своевременному выявлению рецидива. Это особенно важно в рамках контролируемого медикаментозного лечения и подготовки к трансплантации.Обнаружение минимальной остаточной болезни при помощи анализа мутации NPM1 не только улучшает прогнозирование, но и может оказывать влияние на выбор тактики лечения. В частности, позволяет избежать излишне агрессивных препаратов у пациентов с низким риском или, напротив, усилить терапию у тех, кто имеет высокий риск рецидива. Такой персонализированный подход к терапии способствует снижению побочных эффектов и увеличению эффективности лечения.
В медицинском сообществе результаты исследований вызвали повышенный интерес, поскольку демонстрируют, как современные молекулярные технологии способны значительно изменить традиционные подходы к лечению онкогематологических заболеваний. В будущем возможно расширение использования таких методов для контроля других генетических маркеров лейкемии и повышения качества жизни пациентов.Подводя итог, необходимо подчеркнуть, что мутация NPM1 выступает важнейшим молекулярным маркером минимальной остаточной болезни при острой миелоидной лейкемии. Ее выявление в периферической крови после проведения химиотерапии обладает высокой прогностической значимостью для риска рецидива и выживаемости. Клиническая практика, включающая регулярный мониторинг трансриптов мутированного NPM1, позволит своевременно корректировать лечебные стратегии и повысить эффективность применения аллогенной трансплантации стволовых клеток главным образом среди пациентов со стандартным цитогенетическим риском.
Современные молекулярные методы диагностики создают новые возможности для персонализированного лечения и улучшения долгосрочных исходов при острой миелоидной лейкемии.