Память и обучение традиционно ассоциируются с нервной системой — сложной сетью нейронов, которая обеспечивает хранение и обработку информации в мозге. Одним из фундаментальных признаков эффективного обучения является эффект распределённого, или spaced, обучения. Этот феномен описывает ситуацию, когда повторение учебного материала через оптимальные интервалы времени, а не однократное концентрированное повторение (massed learning), приводит к более прочной и долговременной памяти. Данный эффект был впервые описан ещё в XIX веке психофизиологом Германом Эббингаузом и с тех пор стал краеугольным камнем теорий о механизмах памяти как на поведенческом, так и на нейрофизиологическом уровне. Однако недавние прорывные исследования доказывают, что фундаментальные процессы памяти не исключительно нейрональные — они наблюдаются даже в неневральных человеческих клетках, открывая новую эру в понимании клеточной памяти и сигналинга.
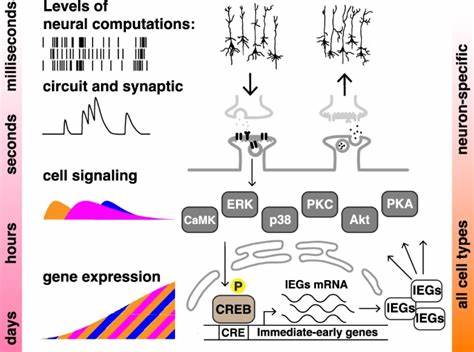
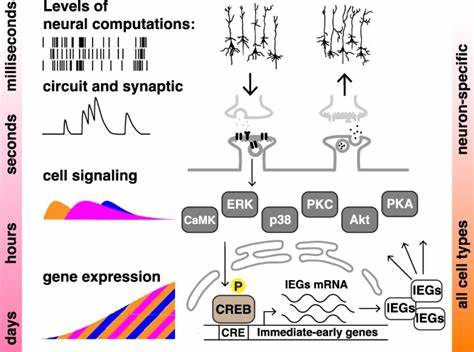
Суть эффекта распределённого обучения сводится к тому, что время между обзорами или тренировками информации играет критическую роль в формировании устойчивых следов памяти. Когда интервал между обучающими сессиями подобран оптимально, молекулярные сигнальные каскады активируются настолько, что создают долговременные изменения в работе клетки, обеспечивая надежное запоминание. При слишком плотном повторении (massed training) эффекты усвоения информации и устойчивость памяти существенно снижаются. Эксперименты, проведённые на нейрональных культурах, показали, что в основе распределённого обучения лежит активация ключевых сигнальных молекул, таких как протеинкиназы А (PKA) и С (PKC), а также киназы ERK и транскрипционного фактора CREB. Однако до недавнего времени считалось, что такой комплекс молекулярных процессов является свойственным исключительно нервным клеткам, особенно учитывая их специфику — синаптическую передачу, нейротрансмиттеры и электрическую возбудимость.
Впечатляющим открытием стало выявление эффекта распределённого обучения в двух типах нелогичных, немозговых человеческих клеток, модифицированных с использованием короткоживущего репортера люциферазы под контролем промотора, зависящего от CREB. Данное исследование имитировало процесс обучения с помощью последовательных импульсных воздействий двух агоністов — форсколина, активирующего PKA через повышение уровня цАМФ, и тетрадеканоила фуроата (TPA), активирующего PKC. В этих системах четырёхкратное воздействие распределёнными во времени импульсами вызывало значительно более сильную и устоявшуюся транскрипционную активность по сравнению с одним концентрированным импульсом. Примечательно, что данное повышенное и длительное увеличение активности было зафиксировано спустя 24 часа после начала воздействия, несмотря на то, что сами стимулы прекращались значительно раньше. Это явно иллюстрирует, что память на клеточном уровне — по крайней мере в части своей молекулярной основы — формируется не просто в результате краткосрочного ответа на стимул, а благодаря сложным механизмам с устойчивой динамикой.
Оценка активации киназы ERK и CREB продемонстрировала, что именно их фосфорилирование интенсивнее при распределённом обучении, чем при массированном. Выявлено, что ингибирование этих молекул приводит к блокировке эффекта распределённого обучения, что подтверждает их ключевую роль как молекулярных детекторов временных паттернов стимуляции. Этот факт указывает на то, что временная организация сигналов — необходимость для формирования долговременной памяти — определяется не только синапсами и нейронной сетью, но и внутриклеточным каскадом, существующим в различных типах клеток. Такое расширенное понимание клеточной памяти позволяет рассматривать обучение как феномен, глубоко укоренившийся в эволюционно консервативных системах клеточного сигналинга, а не исключительно как продукт нервной ткани. Важным элементом исследования стал выбор клеточной линии SH-SY5Y — человеческих нейробластомных клеток, которые, несмотря на происхождение из нервной ткани, обеспечивают удобную основу для изучения молекулярных процессов в контролируемых условиях.
Однако для исключения возможного влияния нейроноподобных особенностей, была также использована линия HEK293 — клеток эмбриональной почки, совершенно не связанных с нервной системой. И в этих клетках наблюдался выраженный эффект spacing, что подчеркивает универсальность данного явления. Изучение воздействия распределённых импульсов активности PKA и PKC открыло глубокие молекулярные зависимости и позволило предположить, что каждая из этих протеинкиназ настроена на определённые интервалы времени (intertrial intervals, ITI), что создаёт сложное перекрытие сигналов при сочетанном воздействии. Это намекает на то, что в организме обучение и адаптация могут возникать из динамического взаимодействия конкурирующих временнЫх окон сигнальной активности, обеспечивая гибкое и точное кодирование информации. Помимо сугубо биохимических наблюдений, исследования выявили, что активированный ERK перемещается в ядро клетки, где инициирует активацию транскрипционных факторов и запускает экспрессию генов, необходимых для долговременных изменений.
И именно эта переработка сигнала во времени в пространстве клетки (цитозоль против ядра) является важным аспектом механизма памяти на уровне клетки. Ключевым в понимании эффекта распределённого обучения также стало осознание не только усиления сигнала, но и замедления его затухания. При повторных, распределённых по времени стимуляциях активность транскрипционного ответа сохраняется более долго, аналогично тому, как распределённое обучение влияет на снижение скорости забывания у животных и людей. Такой временной контур клеточной памяти свидетельствует о наличии механизмов, которые «запоминают» предыдущее воздействие, не требуя при этом сетевой нервной структуры. На молекулярном уровне поддержание длительного ответа может быть обусловлено цикличными положительными обратными связями в каскаде сигналинга, например между ERK и CREB или поддержанием активности протеинкиназ.
Кроме того, возможна роль дополнительных факторов, таких как устойчивое повышение экспрессии самих CREB и других регуляторных белков, что создаёт самоподдерживающийся транскрипционный режим. Это исследование внесло значительный вклад в концепцию «клеточной когниции» — того, что даже отдельная клетка способна к сложной обработке информации и длительному хранению данных о внешних сигналах. Отказ от традиционных представлений о памяти как исключительно нейрональном феномене открывает новые направления в понимании биологического познания и адаптации. Практическое значение открытых закономерностей трудно переоценить. Массовый потенциал такой системы в лабораторных условиях позволяет существенно повысить throughput экспериментов, что крайне ценно для разработки формальных математических моделей памяти и её молекулярных основ.
Это, в свою очередь, может поспособствовать разработке новых подходов к когнитивному улучшению, терапии заболеваний памяти и даже созданию синтетических биологических систем, способных к обучению. Таким образом, эффект распределённого обучения, открытый в неневральных человеческих клетках, показывает, что фундаментальные процессы памяти лежат глубже, чем нервная система, обусловлены консервативными молекулярными механизмами и реализуются посредством временной декодировки химических сигналов. Эта новая перспектива поднимает фундаментальные вопросы о природе памяти и интеллекта, провоцируя переосмысление роли каждой клетки в восприятии, запоминании и реакции на окружающий мир. Будущие исследования в данном направлении обещают раскрыть, каким образом сигнальные сети интегрируют различные временные паттерны, какие ещё молекулярные компоненты участвуют в этих процессах, и как эта информация может быть использована для создания высокоэффективных протоколов обучения и лечения нейродегенеративных заболеваний. Кроме того, изучение таких механизмов в клетках разных типов и организмов позволит лучше понять эволюционные пути появления и усложнения памяти как биологического явления.
В итоге, идея, что память — это монополия нервной ткани, уступает место более всеобъемлющей концепции, где каждая клетка, используя общий молекулярный набор инструментов, способна к сложной обработке информации, надежному хранению и адаптивной реакции. Это фундаментальное переосмысление откроет новые горизонты в биологии, медицине и биотехнологиях будущего.