В последние десятилетия процесс открытия новых лекарственных средств переживает значительные трудности: несмотря на стремительный прогресс в областях высоких технологий и биомедицины, разработка препаратов становится всё более затратной и длительной. Этот феномен получил название "закон Эрумса" - термин, образованный в результате обратной перестановки имени закона Мура, отражающего постоянное удешевление и повышение производительности технологий. В то время как возможности вычислительной техники растут экспоненциально, фармацевтическая отрасль сталкивается с парадоксальной тенденцией: стоимость создания нового лекарства с учётом инфляции удваивается примерно каждые девять лет, а сроки и сложности исследований стремительно увеличиваются.Разобраться в причинах этого явления важно не только для учёных и специалистов, но и для общества в целом, поскольку скорость и эффективность разработки новых препаратов напрямую влияют на здоровье миллионов людей по всему миру. Существует несколько ключевых факторов, которые объясняют возникновение и усиление закона Эрумса.
Первый из них - так называемая проблема "лучше Битлз". Она отражает сложность создания инновационных лекарств, которые должны превосходить уже существующие, широко признанные препараты. Классический пример - популярный и эффективный препарат Липитор, который стал очень популярным благодаря своим характеристикам. На сегодняшний день большинство новых лекарств способны демонстрировать лишь незначительные преимущества по сравнению с уже доступными средствами. Такое положение вещей предъявляет высокие требования к масштабам и сложности клинических испытаний, поскольку малый размер эффекта требует проведения большого числа исследований для статистически достоверного подтверждения эффективности.
Второй фактор связан с ужесточением регулятивных стандартов на фоне случаев серьезных проблем безопасности с препаратами на рынке, например с талидомидом и Виоксом. В результате регуляторные органы снижают свою терпимость к рискам, что ведёт к ужесточению требований к доклиническим и клиническим исследованиям. В конечном итоге это обуславливает значительное увеличение затрат и времени, необходимых для вывода лекарства на рынок. Третий аспект - человеческий фактор, проявляющийся в стремлении компаний и исследовательских групп наращивать затраты на исследования и разработки, порой без должного контроля и эффективности вложений. Такая чрезмерная "денежная инъекция" не всегда приводит к пропорциональному увеличению результата, зачастую способствуя лишь удлинению сроков и росту стоимости проектов.
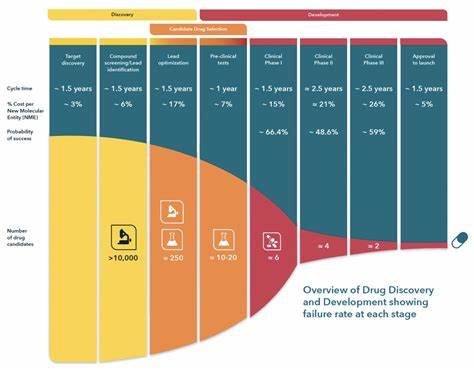
Четвёртый и один из наиболее глубоких факторов связан с эволюцией исследовательских методов в области разработки лекарств. В период с 1960-х по 1990-е годы основной подход строился на тестировании препаратов на цельном организме - фенотипическое скринирование, которое давало более объёмное понимание эффекта новых веществ на биологическую систему. Сейчас же доминируют методы "обратной фармакологии" и целенаправленного поиска, основанные на тестировании взаимодействия веществ с отдельными молекулярными мишенями. Хотя такие методы позволяют ускорить первичный отбор кандидатов и сэкономить средства, они не всегда отражают сложность биологических процессов в организме, что приводит к высокому уровню неудач на более поздних этапах клинических испытаний. Появление и широкое внедрение методов высокопроизводительного скрининга (High-Throughput Screening, HTS), позволяющего одновременно тестировать тысячи соединений, также внесло свою лепту.
Несмотря на свою эффективность и скорость, HTS в некоторых случаях может быть менее продуктивным с позиции конечного результата, так как быстрота отбора зачастую пренебрегает более глубоким пониманием биологической специфики и сложных взаимодействий. Одним из распространённых объяснений замедления развития новых препаратов является представление о том, что "низко висящие плоды" уже собраны - то есть самые очевидные и эффективные лекарственные мишени уже исследованы и использованы. Однако такое заявление не является полностью точным. На самом деле ученые признают существование большого количества потенциальных мишеней и альтернативных подходов, которые ещё недостаточно изучены. Примером может служить исследование так называемых "грязных" или менее селективных препаратов, взаимодействующих с множеством зеркальных мишеней.
Такие лекарственные средства, особенно востребованные в терапии центральной нервной системы, долгое время оставались в тени, но постепенно вызывают вновь повышенный интерес. Помимо внутренних биомедицинских факторoв, на процесс значительно влияет структура самой фармацевтической индустрии. Критики указывают на формирование своеобразной картельной структуры отрасли, где около двадцати крупнейших компаний контролируют большую часть мирового рынка брендированных лекарств с оборотом около триллиона долларов в год. В условиях сниженного уровня конкуренции компании зачастую уменьшают инвестиции в исследования и разработки, предпочтительно увеличивая расходы на маркетинг и рост цен на уже выпускаемые препараты. Такая ситуация усугубляет проблемы инноваций и ведёт к снижению эффективности отрасли в целом.
В последние годы наблюдается интересная тенденция: академические стартапы и небольшие биотехнологические компании выходят на первый план в создании наиболее успешных и высоко продаваемых препаратов. По некоторым оценкам, около 80 процентов таких лекарств в 2018 году появились вне крупной фарм-индустрии. Это указывает на то, что источниками инноваций становятся более гибкие, специализированные структуры, способные применять новые научные знания и технологии с большей эффективностью. Несмотря на все вызовы, связанные с законом Эрумса, развитие биотехнологий, применение методов искусственного интеллекта и машинного обучения, а также современные подходы в генной инженерии и персонализированной медицине создают предпосылки для преодоления нынешних барьеров. Ожидается, что грамотное сочетание новых технологий с реформированием регуляторной политики и устойчивым финансированием научных исследований позволит не просто замедлить негативные тенденции, но и породить новую волну качественных и эффективных лекарств.
В перспективе это будет способствовать не только улучшению здоровья населения, но и развитию всей фармацевтической отрасли, превращая вызовы сегодняшнего времени в драйверы завтра. .