Кора головного мозга — это сложная структура, в которой формируются высокоорганизованные нейронные сети, обеспечивающие все высшие функции нервной системы человека. Именно в коре возникают такие процессы, как мышление, память, восприятие и моторное управление. Однако нарушения в развитии коры могут привести к серьезным заболеваниям, включая мальформации коры, нейродегенеративные и нейропсихиатрические расстройства. Для понимания причин и механизмов возникновения подобных патологий учёные всё чаще прибегают к моделированию ранних стадий развития мозга с использованием человеческих нейрональных стволовых клеток (НСC). Это позволяет пролить свет на молекулярные и клеточные процессы, происходящие ещё на эмбриональном этапе, когда формируется основа коры.
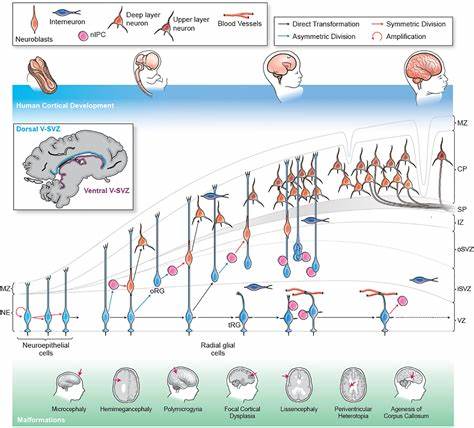
Ранние этапы развития коры мозга формируются в процессе, называемом кортикогенезом, который начинается с активности нейрональных стволовых клеток, известных также как радиальные глиальные клетки. Эти клетки делятся и дифференцируются, давая начало различным типам нейронов и глии. Важную роль в этом процессе играют организаторы мозга, специальные области, которые регулируют пространственно-временную спецификацию стволовых клеток, формируя различные регионы теленцефалона, из которого развивается кора. Сбой в регуляции работы этих стволовых клеток или в сигнальных путях организаторов может вызвать нарушение нормального развития коры, что ведет к возникновению целого спектра корковых нарушений. Современные исследования выявили многочисленные гены, которые ассоциируются с такими заболеваниями, как микроцефалия, лиссэнцефалия, мигрена, мандариновая кортикальная дислазия, а также с нейропсихиатрическими расстройствами, в том числе с аутизмом, шизофренией, биполярным расстройством и расстройствами внимания.
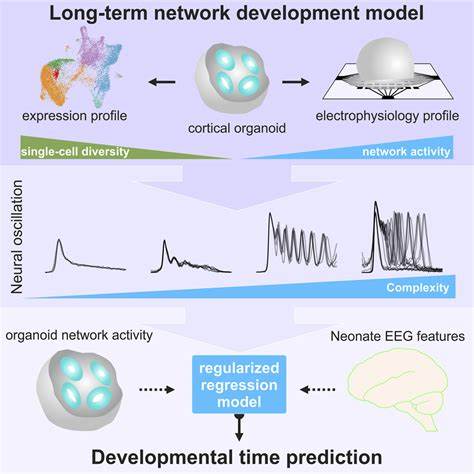
Эти гены экспрессируются на самых ранних этапах развития стволовых клеток, что указывает на важность патогенетических процессов именно в этих стадиях. Благодаря передовым методам, таким как одиночное клеточное транскриптомное секвенирование, стало возможным отслеживать динамику экспрессии этих генов и выявлять критические периоды, когда клетки наиболее чувствительны к нарушениям. Одним из инструментов, широко используемых для изучения раннего развития коры, является культура человеческих нейрональных стволовых клеток, полученных из индуцированных плюрипотентных стволовых клеток (iPSC). Эти культуры могут воспроизводить последовательные этапы дифференцировки клеток, имитируя процессы мозговой органогенеза in vitro. Ученые смогли воспроизвести в таких системах организаторные центры мозга, такие как кортикальный гем и вентральные образования, которые регулируют направленность развития нейрональных линий, что позволяет исследовать влияние тех или иных генетических вариаций на формирование коры.
Данные, полученные из таких моделей, позволяют выявить регуляторные цепочки и сети транскрипционных факторов, влияющих на судьбу клеток, а также понять, каким образом их дисфункция приводит к патологиям. Например, транскрипционные факторы такие как FOXG1, MEIS2, POU3F2 и другие играют ключевую роль в формировании и специализации нейрональных линий, и их нарушения ассоциируются с различными корковыми расстройствами, включая аутизм и другие нейроразвитийные заболевания. Современные биоинформатические подходы позволяют моделировать влияние потери функции отдельных генов или факторов транскрипции на траектории дифференцировки клеток. Виртуальные эксперименты с использованием инструментов анализа мультиомных данных, таких как CellOracle, помогают прогнозировать изменения в клеточных линиях и выявлять особенности, которые могут быть мишенями для терапевтического вмешательства. Особый интерес представляет выявление индивидуальных особенностей развития коры у пациентов с аутизмом и другими нейродегенеративными заболеваниями.
Исследования, в которых используются нейрональные стволовые клетки, полученные от пациентов (персонализированные модели), позволяют обнаружить уникальные паттерны нарушения экспрессии генов и транскрипционных факторов. Это важно для развития прецизионной медицины, нацеленной на лечение конкретных подтипов заболеваний, а также для выявления биомаркеров, потенциально пригодных для ранней диагностики. Международные базы данных и аналитические платформы, такие как NeMO Analytics, предоставляют доступ к обширным наборам данных по развитию мозга, объединяя научные результаты разных групп и упрощая интерпретацию сложной информации. С помощью таких ресурсов исследователи могут сравнивать экспрессию ключевых генов, изучать сетевые взаимодействия и строить модели развития мозга с учетом индивидуальных генетических и молекулярных особенностей. В свете всех этих достижений перспективы лечения корковых нарушений сегодня выглядят многообещающими.
Понимание ранних этапов патогенеза позволит разработать терапевтические стратегии, направленные на коррекцию сбойных процессов еще на стадии нейрональных стволовых клеток. Таким подходом не только возможно предотвратить развитие тяжелых неврологических расстройств, но и помочь пациентам с уже развившимися симптомами улучшить качество жизни. Реализация подобных исследований требует междисциплинарного сотрудничества между биологами, клиницистами, генетиками и специалистами в области биоинформатики. Современные технологии, включая редактирование генов, культивирование трехмерных органоидов и системный анализ данных, создают уникальные возможности для изучения человеческого мозга на самых ранних этапах развития. Таким образом, моделирование ранних стадий развития коры человеческим мозгом с применением нейрональных стволовых клеток является ключевым направлением в исследовании корковых нарушений.
Эти модели помогают раскрывать сложные молекулярные механизмы заболеваний, выявлять критические периоды предрасположенности к патологиям и разрабатывать новые методы диагностики и лечения. Дальнейшее усовершенствование технологий и расширение клинических исследований ускорит переход от фундаментальных открытий к практическим решениям, направленным на снижение бремени корковых и нейроразвитийных заболеваний в обществе.