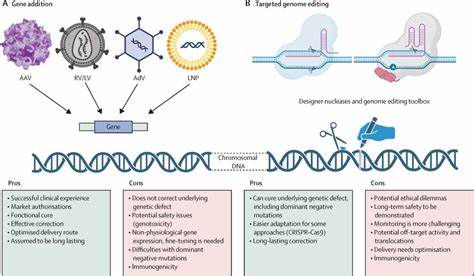
Прецизионное генное редактирование сегодня становится одной из самых значимых и перспективных сфер в области биомедицины. Этот инновационный подход позволяет вносить точечные изменения в ДНК, что открывает беспрецедентные возможности для лечения заболеваний на самом фундаментальном уровне — в генах. В последние годы технологии редактирования генома, такие как base editors и prime editors, сделали качественный скачок и начали менять взгляды на лечение наследственных и приобретённых патологий. Суть прецизионного генного редактирования заключается в возможности вносить специфические изменения в последовательность ДНК без повреждения окружающего геномного материала. Современные методики позволяют исправлять мутации с исключительной точностью, устраняя причины многих генетических заболеваний, ранее считавшихся неизлечимыми.
Примером тому служат базовые редакторы (base editors), способные заменять отдельные нуклеотиды без разрушения двойной спирали ДНК, что значительно снижает риск ошибок и побочных эффектов. В медицинской практике проект активно начинает внедряться в терапии различных болезней, включая наследственные аномалии, редкие генетические патологии и даже некоторые формы рака. Ранние клинические испытания дают обнадёживающие результаты, показывая улучшение состояния пациентов и значительное снижение симптоматики. Благодаря возможности точечного исправления генов появляется надежда на то, что в будущем многие заболевания перестанут быть приговором, а лечение будет максимально персонализировано и эффективным. Тем не менее, несмотря на впечатляющие достижения, технология прецизионного генного редактирования находится пока на этапе становления, и её широкое распространение требует решения ряда серьёзных задач.
Важным вызовом остаётся обеспечение безопасности — несмотря на большую точность, абсолютно исключить риски непреднамеренных мутаций пока невозможно. Также остается необходимым разработка оптимальных методов доставки редакторных систем в клетки организма, чтобы их воздействие было максимально точным и эффективным. Сегодня мир науки активно работает над расширением клинической базы данных, которая позволит понять долгосрочные последствия и потенциал генного редактирования. Научное сообщество ведёт глубокое изучение эффективности этих методик в разных типах тканей, а также исследований по снижению иммунных реакций на внедрённые редакторы. Важно отметить, что помимо технических и биологических вопросов существует и немало этических дилемм, связанных с вмешательством в геном человека, которые требуют общественного обсуждения и законодательного регулирования.
Эксперты считают, что генная медицина будущего будет строиться на принципах интеграции прецизионного редактирования с другими инновационными технологиями, такими как искусственный интеллект и высокоточный анализ больших данных. Это позволит создавать индивидуальные программы лечения на основе полного понимания генетической информации каждого пациента и многочисленных факторов, влияющих на развитие болезни. Кроме того, развитие генного редактирования в комбинации с клеточными технологиями открывает путь к регенеративной медицине на новом уровне. Возможности создания «исправленных» клеток для трансплантации и восстановления функций организма вдохновляют многих учёных и клиницистов на создание революционных терапевтических решений. Перспективы применения прецизионного генного редактирования также связаны с борьбой против инфекционных заболеваний.
Технологии позволяют создавать противомикробные препараты и вакцины, а также модифицировать иммунные клетки пациента для более эффективной борьбы с вирусами и бактериями. Это особенно важно в условиях глобальных эпидемий и появления новых патогенов. Развитие этой области зависит от совместных усилий науки, медицины, этики и законодательства. Необходимы чёткие международные стандарты и протоколы, которые смогут обеспечить безопасность и эффективность новых методов, а также защиту прав пациентов. Важно, чтобы доступ к этим инновационным медицинским решениям был справедливым и доступным для разных слоёв населения.