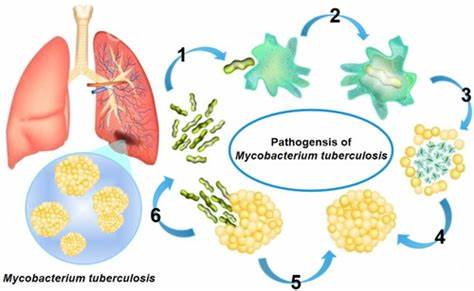
Туберкулёз остаётся одной из самых серьёзных инфекционных угроз для здоровья человечества, несмотря на значительный прогресс в медицине. За последние десятилетия эта болезнь не только не утратила свою актуальность, но и приобрела новые опасности в виде устойчивых к антибиотикам штаммов. Главным виновником коварства туберкулёза является бактерия Mycobacterium tuberculosis, отличающаяся уникальными защитными механизмами, которые осложняют создание и применение эффективных лекарств. Одной из сложнейших задач в противодействии туберкулезу является проницаемость лекарственных препаратов сквозь многоуровневую клеточную оболочку микобактерий. Структура клеточной стенки этих бактерий не похожа ни на грамположительные, ни на грамотрицательные бактерии, обладая своей особой многоступенчатой "бронёй".
В основе лежит клеточная мембрана, вокруг которой располагается периплазматическое пространство, покрытое слоем пептидогликана. За ним следует уникальный слой арабиногликана, а завершает эту структуру двойной слой миколовой кислоты с разнообразными липидами и белками на поверхности. Такое сложное строение не просто препятствует проникновению лекарственных веществ внутрь клетки, но и обеспечивает высокую устойчивость бактерии к воздействию иммунной системы хозяина. Макрофаги - клетки иммунной системы, ответственные за уничтожение патогенов - сталкиваются с серьёзными сложностями при попытке избавиться от микобактерий именно из-за этой липидной оболочки, которая защищает патоген внутри клеток легких, позволяя бактерии медленно, но уверенно развиваться. Рост Mycobacterium tuberculosis происходит крайне медленно, что само по себе представляет определённую сложность для диагностики и терапии.
В лабораторных условиях колонии бактерий могут формироваться в течение нескольких недель, что отягощает своевременное выявление и начало лечения. Латентное состояние инфекции, в котором бактерия может длительно находиться в лёгочной ткани без активации, присутствует примерно у трети населения Земли, что создаёт огромный резервуар потенциальных пациентов. Антибиотики, использующиеся до сих пор для лечения туберкулёза, оказываются всё менее эффективными из-за появления устойчивых штаммов. Особенно тревожным является распространение таких штаммов в ограниченных условиях, вроде тюремных учреждений, где условия способствуют быстрой передаче инфекций и селекции резистентных форм. Постоянное увеличение числа стран с отмеченной антибиотикорезистентностью делает поиск новых, более эффективных препаратов задачей международного здравоохранения.
Современные научные исследования сосредоточены на понимании химических и структурных особенностей молекул, способных преодолевать сложные барьеры микобактерий. Одним из перспективных направлений является применение структурированных пептидов, обладающих способностью проникать через оболочку бактерий. Ранее считалось, что для успешного проникновения необходимы маленькие и гидрофобные молекулы, однако последние открытия показывают, что и пептиды могут справляться с задачей, особенно если они модифицированы по определённым принципам. Модификация пептидов за счет циклизации, то есть создания кольцевой структуры, значительно повышает их эффективность. Важно правильно подбирать размер кольца и типы звеньев, соединяющих его, так как именно такие параметры не только влияют на стабильность молекулы, но и на её способность взаимодействовать с липидными слоями микобактерий.
Также N-метилирование пептидов является важной техникой повышения активности, хотя механизмы его воздействия всё ещё изучаются. Конкретные исследования подтверждают, что применение таких модифицированных пептидов улучшает свойства кандидатов в антибиотики. Один из примеров - изменение структуры антибиотика гризелимицин, особенности циклизации и замещения аминокислот оказались критичными для сохранения и повышения антимикробной активности. Удаление этих элементов значительно снижало эффективность препарата, что подчёркивает важность структурных инноваций в фармакологии. Опасность туберкулёза усугубляется тем, что он распространяется медленными темпами, из-за чего общество иногда недооценивает масштаб проблемы.
В отличие от быстротекущих вирусных инфекций, туберкулёз развивается постепенно, но при этом может привести к масштабным эпидемиям в долгосрочной перспективе. Комбинация высокой устойчивости бактерий к препаратам и большого числа латентно инфицированных людей создает устойчивый очаг инфекции, контроль над которым требует новых подходов и постоянного развития фармакологической базы. Не менее важен комплексный подход, включающий не только разработку новых антибиотиков, но и совершенствование методов диагностики, профилактики и общественного здравоохранения. Повышение осведомленности, укрепление систем выявления и изоляции больных, а также строгое соблюдение схем лечения - ключевые элементы борьбы с распространением болезни. Вклад фундаментальных исследований в области биохимии и молекулярной биологии микобактерий помогает найти новые мишени для лекарств.
Изучение физиологических особенностей бактерий, их взаимодействия с иммунными клетками, а также механизмов защиты от лекарственных средств дает надежду на создание инновационных препаратов. Также ведутся работы по использованию нанотехнологий и биоспецифичных доставляющих систем, способных точно направлять лекарственные вещества непосредственно к очагу инфекции. Таким образом, борьба с туберкулёзом требует не только усилий медицинского сообщества, но и координации научных, общественных и политических структур. Инвестиции в исследования, разработка эффективных стратегий лечения, а также внедрение современных технологий в клиническую практику - это фундаментальные шаги на пути к снижению бремени этого заболевания в мире. Туберкулёз - не просто медицинская проблема, но и социально-экономический вызов, тесно связанный с условиями жизни, доступом к медицинской помощи и глобальной мобильностью населения.
Современные успехи в понимании защитных механизмов микобактерий вселяют надежду на прорыв в создании новых лекарственных средств, которые смогут эффективно преодолевать толстую оболочку бактерий и вести к полной ликвидации инфекции. Итогом можно считать, что борьба с туберкулёзом - это комплексная задача, требующая глубоких научных знаний о структуре и поведении возбудителя, современных методов разработки и модификации лекарств, а также постоянного мониторинга и адаптации терапевтических стратегий с учетом меняющейся картины антибиотикорезистентности. Только в таком ключе можно рассчитывать на успешное снижение глобальной нагрузки от туберкулёза и защитить здоровье миллионов людей по всему миру. .