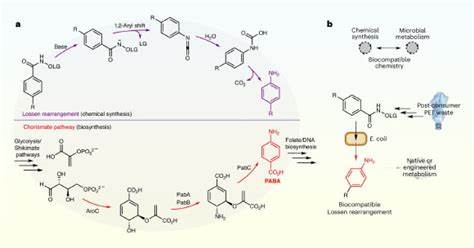
В последние годы биосовместимая химия приобретает все большее значение благодаря своей способности соединять достижения органического синтеза с живыми системами. Одним из прорывных достижений в этой области стала реализация биосовместимой реакции перераспределения Лоссена в бактерии Escherichia coli. Этот подход позволяет проводить химическую трансформацию, традиционно недоступную для биологических систем, прямо внутри живых клеток, что открывает новые горизонты в устойчивом биосинтезе и переработке отходов. Реакция Лоссена, открытая еще в XIX веке, представляет собой превращение активированных гидроксаматов в первичные амины через 1,2-ароматический миграционный механизм с образованием промежуточного изоцианата. Несмотря на широко известный синтетический потенциал этой реакции, ее интеграция с клеточным метаболизмом до недавнего времени оставалась неизвестной, поскольку она требует специфических условий и катализаторов, не всегда совместимых с жизнедеятельностью микроорганизмов.
Исследователи смогли преодолеть эти ограничения, обнаружив, что в среде, содержащей фосфаты, реакция перераспределения Лоссена протекает спонтанно и без токсичности для Escherichia coli. Фосфатные ионы выполняют роль эффективного катализатора, обеспечивая мягкие условия реакции при нейтральном pH и температуре, совместимой с жизнью бактерий. Такое открытие доказывает многофункциональную роль фосфатов в клеточных процессах, расширяя их значение от классической регуляции рН и синтеза мембран до катализа органических реакций внутри клетки. В биологических системах первичные амины играют критическую роль, выступая в качестве строительных блоков для многочисленных метаболитов и биомолекул, включая аминокислоты, нейротрансмиттеры и витаминные компоненты. Традиционно пути их биосинтеза ограничены специфическими ферментами, такими как аминотрансферазы и аммониум-лиазы.
Реакция перераспределения Лоссена обеспечивает альтернативный, неэнзиматический путь образования аминов, что расширяет синтетический потенциал микроорганизмов и открывает новые возможности для метаболического инжиниринга. Чтобы продемонстрировать практическую применимость этой реакции, ученые использовали штамм Escherichia coli с дефицитом по пара-аминобензойной кислоте (ПАБК) — ключевого метаболита для биосинтеза фолиевой кислоты и, как следствие, нуклеотидов. В условиях отсутствия ПАБК рост бактерий невозможен. С помощью перераспределения Лоссена из специально синтезированного гидроксамата, являющегося предшественником ПАБК, рост микроорганизмов был успешно восстановлен — продемонстрировав, что реакция эффективно протекает in vivo и генерирует жизненно важные метаболиты. Особое внимание в исследовании уделялось синтезу предшественника перераспределения Лоссена из полиэтилентерефталата (ПЭТ) — широко распространенного пластика, составляющего значительную часть мировых отходов.
Это открывает перспективы биосредств для утилизации и апсайклинга пластиковых материалов. Гидролиз ПЭТ приводит к образованию терефталевой кислоты, которая затем была преобразована в активированный гидроксамат. Введение этого соединения в культуру E. coli позволило выращивать бактерии, зависимые от ПАБК, тем самым превращая пластиковые отходы в биомассу посредством цепочки биохимических реакций. Кроме того, реакция перераспределения Лоссена была интегрирована с природными и синтетическими метаболическими путями бактерии для производства промышленных молекул, таких как парацетамол.
В нескольких этапах реакции гидроксамат превращается в ПАБК, который метаболически преобразуется в 4-аминофенол и далее ферментативно ацетилируется в парацетамол — широко используемое обезболивающее и жаропонижающее средство. Такой биотехнологический процесс позволяет синтезировать лекарство непосредственно из пластиковых отходов, предоставляя экологически значимую альтернативу традиционному химическому производству с использованием невозобновляемых ресурсов. Интеграция неэнзиматической реакции с живыми клетками требует соблюдения баланса между реакционной эффективностью и биосовместимостью. В случае перераспределения Лоссена, реакция была оптимизирована при использовании фосфатных буферов и контроле параметров среды, что обеспечило минимальное токсическое воздействие и максимальную продуктивность. Это подтверждает важность системного подхода при развитии биосовместимой химии, где особенности микробиологии и химического синтеза должны гармонично сочетаться.
Результаты исследований открывают широкий спектр потенциальных приложений. Биосовместимые реакции могут расширить инструментарий метаболического инжиниринга, позволяя создавать новые метаболиты и химические соединения, которые ранее были недоступны через ферментативные пути. Кроме того, возможности по утилизации и апсайклингу пластиковых отходов на основе природных микроорганизмов могут кардинально изменить подходы к управлению пластиковыми загрязнениями, снижая экологический след производства и отходов. В будущем предстоит углубленное изучение молекулярных механизмов катализируемой фосфатом реакции перераспределения Лоссена, а также разработка новых биосовместимых химических трансформаций для дальнейшего расширения функционального потенциала живых систем. Применение синтетической биологии и направленной эволюции ферментов может способствовать созданию специализированных микроорганизмов с запрограммированными химическими реакциями, что приблизит нас к революционной биохимической производственной платформе.
Таким образом, биосовместимая реакция перераспределения Лоссена в Escherichia coli символизирует важный шаг в создании гибридных биохимико-химических процессов. Эта технология сочетает в себе устойчивость биологических систем и мощь современной органической химии, предлагая эффективные решения глобальных проблем устойчивого производства, биоремедиации и создания высокоценных химикатов из возобновляемых источников и отходов. Исследования в данной области обещают значительное воздействие на экологическую биотехнологию и фармацевтическую промышленность, открывая путь к инновационным технологиям будущего.