Природа наделила живые организмы удивительным набором химических реакций, которые обеспечивают базовые процессы жизнедеятельности. Однако возможности этих реакций ограничены, особенно если речь идет о синтезе новых соединений, необходимых для промышленности и медицины. Современная органическая химия обладает широким спектром реакций, многие из которых не встречаются в природе и называются абиотическими. Слияние таких новых реакций с живыми системами представляет собой перспективное направление, способное привести к более устойчивому производству химикатов и лекарств на основе возобновляемого сырья. Одним из таких прорывов стала биосовместимая версия известной реакции Лоссена, впервые расширяющая возможности бактерии Escherichia coli в синтезе аминсодержащих метаболитов прямо в клетках.
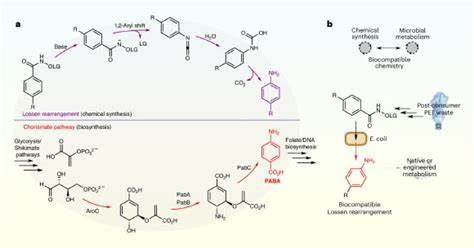
Результат такого взаимодействия — новый инструмент в метаболическом инжиниринге и биокатализе. Реакция Лоссена была открыта в XIX веке и традиционно используется для преобразования акрилгидроксаматов в первичные амины через механизм 1,2-ароматического миграционного сдвига с образованием изоцианатов и последующим гидролизом. Её значимым преимуществом является возможность получения аминов из легко доступных карбоновых кислот без необходимости использования азидов — токсичных и взрывоопасных реагентов, которыми часто сопровождается родственная реакция Куртиуса. Несмотря на свою эффективность в синтетической органической химии, до недавнего времени реакция Лоссена не считалась реализуемой в живых клетках. Уникальное исследование, проведённое международной командой учёных, продемонстрировало, что реакция Лоссена может протекать непосредственно внутри живых клеток кишечной палочки Escherichia coli в присутствии фосфатного катализатора.
Это открывает перспективу для интеграции нового типа химической трансформации с метаболизмом микроорганизмов. В частности, преобразование активированных гидроксаматов в первичные амины, такие как пара-аминобензойная кислота (PABA), жизненно важный метаболит, необходимый для биосинтеза фолиевой кислоты и роста бактерий, позволило управлять ростом бактерий с помощью химического сигнала, привязанного к специфическому химическому субстрату. Важным этапом экспериментов стало использование так называемого auxotroph rescue — метода, при котором бактерии, неспособные синтезировать определённый метаболит, могут выживать только при его внешнем добавлении. В данном случае штаммы Escherichia coli с нарушением синтеза PABA могли восстановить жизнедеятельность при добавлении субстратов, которые в условиях внутри клетки подвергались реакции Лоссена с образованием PABA. Растущие культуры бактерий подтверждали успешность реакции и её биосовместимость, подчеркивая, что химическая трансформация протекала без токсического воздействия на клетки.
Ключевую роль в катализе реакции показала фосфатная буферная система, широко распространенная в биологических средах. Фосфаты, присутствующие в насыщенной среде или внутри клеток, эффективно запускали реакцию при нейтральном pH и температуре около 37°C. Работа эксперимента показала, что реакция происходила и в отсутствии экстенсивных металлоорганических каталитических систем, что значительно упрощает её применение в биотехнологии и снижает потенциальные вредные воздействия на микробную среду. Помимо фундаментального открытия, исследование имеет огромное практическое значение в области биоутилизации. Исходный субстрат для реакции Лоссена может быть получен из терефталевой кислоты, которая является мономером полиэтилентерефталата (PET) — одного из наиболее распространённых видов пластиковых отходов.
Синтез гидроксаматов из PET позволяет превратить нераспадающийся пластик в полезные химические соединения, интегрируемые в метаболизм бактерий. Таким образом, создан уникальный подход к биоремедиации пластика — превращению пластика в питательные вещества, обеспечивающие рост микробных культур. Эксперименты показали, что субстрат, созданный из переработанного пластикового материала, полноценно поддерживал рост PABA-ауктотрофного штамма Escherichia coli. Это доказывает возможность использования искусственно созданных бактерий для биоконвертации пластиковых отходов в биомассу и биопродукты, что способствует экологически чистым технологиям обращения с пластиком и сокращению загрязнения окружающей среды. Ещё один значимый аспект исследования — успешное сочетание биосовместимой реакции Лоссена с другими ферментативными процессами в клетках Escherichia coli для синтеза ценных фармацевтических соединений.
Так, пара-аминобензойная кислота, образуемая в ходе реакции, была промежуточным звеном в биосинтезе парацетамола — широко применяемого анальгетика и жаропонижающего препарата. Для этого были внедрены бактериальные штаммы с экспрессией ферментов, превращающих PABA сначала в 4-аминодифенол, а затем — в парацетамол, что было показано при инкубации клеток с субстратом гидроксаматов. Такой биокаталитический каскад, сочетающий абиотическую (неферментативную) химию с ферментативными биохимическими реакциями, продемонстрировал мощную платформу для синтеза лекарств из пластикового сырья, что представляет собой уникальное достижение в мире биотехнологии. На сегодняшний день производство парацетамола осуществляется по энергоемким промышленным путям с использованием нефтехимических предшественников. Новая биосовместимая технология открывает путь к более устойчивому производству медикаментов, сокращая зависимость от невозобновляемых ресурсов и снижая экологический след производства.
Кроме получения PABA и парацетамола, исследователи продемонстрировали, что биосовместимая реакция Лоссена может контролировать другие биокаталитические процессы, такие как восстановление двойных связей в алькенах, что расширяет химический репертуар живых клеток и возможности создания новых химических продуктов с помощью биокатализа. Эта инновационная работа иллюстрирует, как объединение современной органической химии с биотехнологией и синтетической биологией может привести к созданию новых устойчивых решений. Возможность реализации новых типов реакций внутри живых клеток не только расширяет возможные химические трансформации, но и открывает перспективы для переработки отходов, производства биоактивных веществ и управления метаболизмом. В целом, биосовместимая реакция Лоссена в Escherichia coli — это важный шаг на пути к интеграции абиотических химических процессов с биологическими системами. Она демонстрирует, что бактерии могут использоваться не только как фабрики по синтезу классических биомолекул, но и как универсальные платформы для реализации сложных химических реакций, недоступных ранее в природе.
Подобные технологии обещают революционизировать области биопроизводства, экологической химии и фармацевтики. В перспективе дальнейшие исследования будут направлены на оптимизацию условия работы реакции внутри клеток, улучшение выхода и специфичности реакций, а также расширение спектра биосовместимых реакций и их применение в различных микроорганизмах. Интеграция таких химических процессов в промышленные биотехнологические производства может значительно снизить экологическую нагрузку, повысить эффективность утилизации пластика и сделать производство лекарств более доступным и зеленым. Таким образом, открытие и развитие биосовместимой реакции Лоссена открывает двери новой эре устойчивой химии, где природные механизмы и искусственные химические подходы объединяются для создания умных биокаталитических процессов, полезных не только для науки, но и для решения острых экологических и медико-промышленных задач.