Кетамин - это уникальное вещество, которое начало использоваться в медицине ещё в XX веке как анестетик, но в последние годы привлекает повышенное внимание благодаря своим необычным психотропным свойствам и быстрому антидепрессивному эффекту. Его действие на мозг человека сложно переоценить, так как оно затрагивает как нейрохимические процессы, так и работу различных мозговых сетей, отвечающих за эмоции, восприятие и мышление. Понимание того, как кетамин работает в мозге и почему он способен изменять сознание и мыслительные процессы, имеет важное значение для разработки новых технологий лечения психических расстройств. Основным фармакологическим механизмом кетамина является блокировка NMDA-рецепторов - специфических белков на поверхности нейронов, которые отвечают за передачу сигналов с участием глутамата, основного возбуждающего нейромедиатора в коре головного мозга. Кетамин представляет собой рацемическую смесь двух зеркальных форм - R- и S-энантиомеров, при этом их фармакодинамические свойства отличаются.
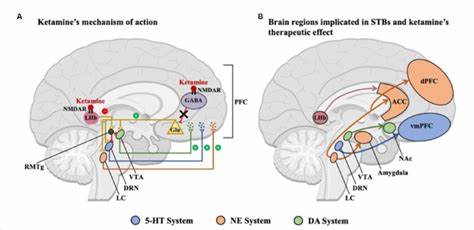
В субанестетических дозах, то есть при дозировках ниже тех, что вызывают полную анестезию, вещество блокирует NMDA-рецепторы именно на кортикальных интернейронах, тормозящих активность пирамидальных нейронов. Такая блокировка ведёт к снижению ингибирующего действия интернейронов ГАМК (гамма-аминомасляной кислоты), что называется гипотезой дисинhibition - "раздискретизации" нейронов. В результате пирамидальные нейроны выходят из-под подавления, происходит резкий подъём выброса глутамата, который активирует другие рецепторы - АМРА, вызывая приток кальция в постсинаптическую клетку. Этот каскад запускает выделение нейротрофического фактора мозга (BDNF) и активацию специфических рецепторов TrkB. Далее цепочка внутриклеточных сигналов приводит к активации mTOR-сигнального пути и других важных молекулярных механизмов, таких как MAPK, PLC-γ и PI3K-Akt, что стимулирует синтез новых синапсов и повышает нейропластичность.
Именно эти процессы обеспечивают быстрое и продолжительное облегчение депрессивных симптомов после инъекций кетамина. Помимо NMDA-блокировки кетамин воздействует и на другие нейрохимические системы. Он способен увеличивать уровни моноаминов - дофамина, серотонина и норадреналина, что дополнительно влияет на настроение и когнитивные функции. При этом R-энантиомер кетамина (аркетамин) проявляет менее выраженные психотомиметические эффекты и может способствовать долгосрочным антидепрессивным эффектам за счёт влияния на сигнальные пути, связанные с ранним геном роста (EGR1) в префронтальной коре, хотя эта область исследований пока остаётся недостаточно изученной. На уровне восприятия и сознания кетамин проявляет себя как диссоциативный анестетик.
При высоких дозах он вызывает седативный эффект и обезболивание, не нарушая при этом функцию сердечно-сосудистой системы, что выгодно отличает его от многих других анестетиков. При субанестетических дозах пациенты часто испытывают состояния деперсонализации и дереализации, искажение восприятия времени, яркие образы и галлюцинации. Эти феномены связаны с изменениями в работе кортикальных и лимбических мозговых структур. Современные нейровизуализационные исследования выявляют, что кетамин значительно меняет функциональную связность ключевых областей мозга, участвующих в регуляции настроения и когнитивных процессов. Например, в 2023 году было проведено двойное слепое, плацебо-контролируемое исследование с использованием функциональной магнитно-резонансной томографии, где изучалась связность передней поясной коры (ACC).
У пациентов с резистентной депрессией кетамин специфически модулировал связь подрегенуарной, перигенуарной и дорсальной зон ACC с правой островковой корой и передней вентромедиальной префронтальной корой. Изменения в связности перигенуарной области ACC с островковой корой коррелировали с улучшением клинических показателей депрессии, а также с уменьшением анедонии - неспособности испытывать удовольствие. Дальнейшие исследования показали, что исходный уровень связности между префронтальной корой и лимбической системой может предсказывать ответ пациента на терапию кетамином. У людей с более низкой исходной фронтолимбической связностью отмечалась более выраженная реакция на лечение, сопровождавшаяся усилением нейронных связей, что связано со снижением тяжести депрессии. Эти эффекты явно отличались от изменений, наблюдавшихся у лиц, получавших плацебо, и указывают на уникальный нейрофизиологический механизм действия препарата.
Другое интересное наблюдение касается состояния диссоциации, которое сопровождает приём кетамина. Исследования показали, что различные варианты диссоциативного опыта оказывают различное воздействие на эмоциональную обработку в мозге. При лёгкой деперсонализации активность правой передней островковой коры снижается, что способствует уменьшению негативных эмоций и облегчению неприятных ощущений. Напротив, при диссоциативной амнезии активность островковой коры увеличивается, что может усиливать негативный аффект. Таким образом, не все субъективные состояния приёма кетамина одинаковы, и они по-разному влияют на эмоциональные мозговые цепи.
Важным аспектом действия кетамина является его влияние на латеральное габенулярное ядро - область, играющую роль в негативной регуляции мотивации и награды. Предклинические исследования выявили, что кетамин снижает патологическую гиперактивность этой зоны, что ведёт к устранению признаков "анти-наградной" активности и позволяет дофаминергическим системам по-новому воспринимать стимулы, восстанавливая нормальную обработку положительных эмоций. Это явление может объяснять изменение мышления и чувство отстранённости от привычных негативных мыслей, часто наблюдаемое у пациентов после терапии. С точки зрения когнитивных функций, кратковременное влияние кетамина проявляется в виде временного ухудшения внимания, исполнительных функций и вербальной памяти, но эти изменения, как правило, полностью компенсируются в течение суток. Рабочая память при этом не затрагивается.
Более масштабные метаанализы подтвердили отсутствие устойчивого когнитивного снижения у пациентов, проходивших терапию кетамином, хотя отмечается значительная вариабельность данных и необходимость контроля за возможными побочными эффектами. Повторные курсы инъекций кетамина могут способствовать улучшению обработки информации и памяти, что в большей степени связано с устранением депрессивных симптомов, чем с прямым нейробиологическим воздействием препарата. Клинические исследования демонстрируют, что уже после нескольких инфузий процессы нейропластичности и укрепления синаптических связей ведут к заметной нормализации мозговых функций у пациентов с депрессией. Клиническое применение кетамина в психиатрии быстро развивается. Численные исследования подтверждают эффективность курса из шести инфузий, который обеспечивает высокие показатели ответа и ремиссии у пациентов с леченой депрессией, при этом эффект наступает уже в течение нескольких часов и сохраняется в течение нескольких дней.
По сравнению с традиционной электросудорожной терапией, кетамин характеризуется лучшей переносимостью и безопасностью. Разработаны также и одобрены к применению формы интраназального esketamine, расширяя терапевтические возможности. Несмотря на впечатляющие результаты, необходимо помнить о потенциальных рисках. Острые побочные действия кетамина включают в себя диссоциацию, галлюцинации, повышение артериального давления и тошноту. При хроническом несанкционированном употреблении появляются риски когнитивных нарушений, повреждения мочевого пузыря и зависимости.
Долгосрочная безопасность при повторном медицинском применении остаётся предметом активных исследований, подчёркивая важность строжайшего контроля и наблюдения. Механизмы действия кетамина затрагивают сложные и многоуровневые процессы, и полное понимание всех нюансов пока не достигнуто. Большинство данных получено на основе небольших выборок пациентов и гетерогенной популяции, что усложняет поиск универсальных предикторов ответа на лечение. В перспективе необходимы крупномасштабные исследования с интеграцией данных функциональной нейровизуализации, электрофизиологии и молекулярных биомаркеров для расширения знаний. Итогом можно считать, что кетамин является мощным средством, которое работает за счет блокировки NMDA-рецепторов, вызывая цепочку нейрохимических и структурных изменений в мозге.
Эти изменения проявляются в перераспределении активности ключевых мозговых сетей настроения и вознаграждения, что приводит к быстрому облегчению депрессивных симптомов и изменению восприятия. Кратковременные когнитивные побочные эффекты почти полностью обратимы, а диссоциативные состояния могут выступать не только как побочные явления, но и как посредники терапевтического действия. Будущее применение кетамина требует осторожности и мониторинга, при этом потенциал этого вещества открывает новые горизонты в лечении тяжелых психических заболеваний, трудноподдающихся стандартным методам терапии. .