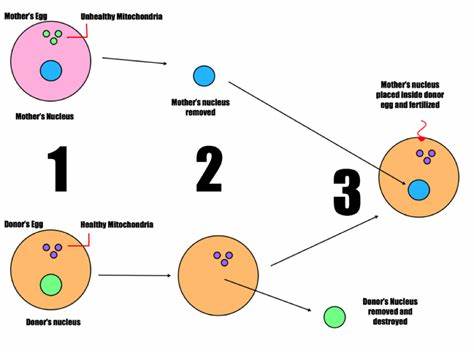
Наследственные митохондриальные заболевания на протяжении десятилетий представляли собой непреодолимую медицинскую проблему для множества семей по всему миру. Эти редкие, но зачастую фатальные генетические патологии передаются от матери к ребенку через митохондриальную ДНК и могут вызывать тяжелые нарушения в работе организма вплоть до паралича, сердечной недостаточности, мозговых повреждений и слепоты. Традиционно для таких семей единственным выходом оставалась суррогатная мать или прием ребенка на воспитание. Однако последние достижения в области генетики и репродуктивных технологий открывают новый перспективный путь для предотвращения этого рода заболеваний – методику с использованием ДНК третьего родителя, известную как митохондриальная донорская терапия или трёхродительское оплодотворение. Суть этой инновационной технологии заключается в замене поврежденной митохондриальной ДНК в яйцеклетке матери на здоровую митохондриальную ДНК донора.
При этом ядро клетки с основным генетическим материалом, ответственным за большинство наследуемых признаков ребенка, берется у родителей, мечтающих о здоровом потомстве. Затем это ядро пересаживается в донорскую яйцеклетку, из которой предварительно удалена дефектная митохондриальная ДНК, после чего эмбрион имплантируется в организм женщины. В итоге ребенок получает генетический материал от трех людей – основное ДНК от родителей и небольшой, но жизненно важный набор митохондриальной ДНК от донора, что позволяет предотвратить развитие тяжелых заболеваний без утраты генетической связи с родителями. Британские ученые, которые на протяжении более десяти лет совершенствовали методику, недавно достигли значимых успехов. В рамках клинических исследований семь матерей с высоким риском передачи митохондриальных заболеваний на свет появились восемь здоровых детей – мальчиков и девочек в возрасте от нескольких месяцев до двух лет.
Данные малыши растут без признаков генетических нарушений, и пока отсутствуют доказательства побочных эффектов или негативных последствий такого вмешательства. Эти результаты признаны мировым научным сообществом и врачами как прорыв в репродуктивной медицине, дающий надежду десяткам тысяч семей по всему миру. Несмотря на успехи, технология вызывает обстоятельные этические и биологические дискуссии. В частности, критики опасаются, что вмешательство в генетический состав будущих поколений несет риски появления нежелательных мутаций, которые могут передаваться дальше по наследству и повлиять на здоровье потомков. Также существуют опасения по поводу будущих возможностей генетической манипуляции, включая реализацию сценариев создания «дизайнерских детей» с целенаправленным изменением наследуемых признаков, что ставит общество перед серьезными моральными дилеммами.
Высказывается опасение и по поводу расширения применения технологии за пределы предотвращения наследственных болезней, например, для борьбы с бесплодием или даже модификации человеческого генома с целью улучшения определенных качеств ребенка. Такие перспективы вызывают справедливые тревоги специалистов и философов по поводу границ научных возможностей и итогов их воздействия на человечество. Тем не менее, сторонники метода подчеркивают, что митохондриальная донорская терапия принципиально отличается от генного редактирования, такого как технологии CRISPR. Здесь решается четкая медицинская задача – избавить детей от страданий и тяжелых последствий болезней, не стимулируя создание модифицированных генов с неясными последствиями. Разные страны по-разному относятся к применению этой технологии.
В Великобритании она легализована и регулируется строгими нормативными актами, которые предусматривают множество контрольных этапов и гарантируют максимальную безопасность для родителей и детей. В США в настоящее время подобные процедуры запрещены, хотя в 2016 году был зафиксирован случай рождения ребенка при использовании подобных техник в Мексике для семьи из Иордании. Такие страны, как Австралия, Греция и Украина, также используют метод для помощи семьям с проблемами митохондриальных заболеваний или даже для борьбы с бесплодием. Стоит особо отметить, что развитие данной технологии меняет восприятие генетической уникальности и семейных отношений. Некоторые исследователи и этические эксперты указывают на необходимость переосмысления значения «собственного» генетического материала и стремления к чистоте генома, предлагая рассматривать новые формы родства и биологической связи шире и более гибко.
Кроме того, для женщин с риском передачи митохондриальных заболеваний доступны и другие варианты, например, усыновление, и каждый случай требует индивидуального подхода и взвешенного выбора. Продолжающееся наблюдение за здоровьем и развитием детей, рожденных с применением технологии «трех родителей», а также тщательные долгосрочные исследования жизнеспособности и безопасности методики помогут сформировать глобальные стандарты и рекомендации, а также проложить путь к более широкому внедрению технологии. Здравоохранительные службы многих стран уже активно обсуждают возможность интеграции методики в программы репродуктивной помощи, что может существенно снизить бремя наследственных болезней и улучшить качество жизни будущих поколений. В конечном счете, использование ДНК третьего родителя открывает уникальные возможности для предупреждения наследственных митохондриальных заболеваний. Это не только технология медицины будущего, но и шаг к гуманной и эффективной помощи семьям, столкнувшимся с тяжелыми генетическими патологиями.
Несмотря на несомненные вызовы и сложные этические вопросы, направления развития и совершенствования методики обещают значительные улучшения в здоровье детей и расширение репродуктивных возможностей. Современный мир становится свидетелем того, как наука меняет понятие наследственности, позволяя сотворить жизнь без тяжелых генетических страданий, что по праву можно назвать медицинским прорывом столетия.