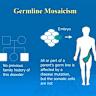
Соматическая мозаичность — явление, при котором в пределах одного организма генетический материал клеток отличается, является ключевым аспектом современной геномной науки. В отличие от наследуемых мутаций, которые передаются от родителей к потомкам с рождения, соматические мутации возникают после оплодотворения и присутствуют лишь в отдельных клетках или клонах клеток организма. Их изучение позволяет понять, как генетическое разнообразие развивается внутри человеческого тела и как оно влияет на здоровье, старение и развитие болезней. Сеть Somatic Mosaicism across Human Tissues (SMaHT), запущенная под эгидой Национального института здравоохранения США, представляет собой масштабный международный проект, направленный на систематический сбор и анализ данных о соматических мутациях в 19 различных тканях от 150 здоровых доноров. Исследователи планируют создать уникальный справочный каталог, охватывающий широкий спектр генетических вариаций и их клональных паттернов, от ранних эмбриональных мутаций до поздних появлений в течение жизни.
Понимание роли соматических мутаций в биологии человека существенно ограничивалось технологическими трудностями. Мутации часто возникают в небольшом числе клеток, поэтому их выявление требовало высокочувствительных методов секвенирования с низкой погрешностью. В рамках SMaHT применяются инновационные технологии, включая глубокое короткочитное секвенирование генома с покрытием более 300×, длительное секвенирование с длинными ридами, а также методики дуплексного секвенирования, значительно снижающие уровень ошибок. Это открывает возможности для выявления редких, ранее недоступных мутаций. Исследования показывают, что с момента оплодотворения и в течение всего жизненного цикла клетки неизбежно накапливают мутации в ДНК.
Некоторые из них обусловлены внутренними ошибками репликации, другие возникают под воздействием внешних факторов, таких как УФ-излучение, канцерогены или воспалительные процессы. В здоровых тканях преобладают однонуклеотидные замены и небольшие вставки или делеции. Структурные варианты генома, включая большие хромосомные перестройки и мобильные элементы, встречаются реже, но обладают потенциалом оказать более глубокое влияние на функцию клеток. Степень соматической мозаичности и скорость появления мутаций зависят от типа ткани и стадии развития. Эмбриональные клетки подвергаются более высокой нагрузке мутаций во время быстрых делений, особенно на ранних этапах формирования зиготы и зародыша.
У взрослого человека частота мутаций варьируется: в постмитотических клетках нервной ткани она составляет около 16–20 однонуклеотидных замен в год, тогда как в эпителии толстой кишки этот показатель может достигать 40–44 замен в год. Такие различия отражают особенности клеточного цикла, регенерации и воздействия окружающей среды. Немаловажно и то, что некоторые соматические мутации способствуют селекции и клонированию клеток с определёнными преимуществами. Например, мутации в генах, связанных с регуляцией роста и выживания, могут приводить к расширению клонов — процессу, аналогичному ранним этапам канцерогенеза, но при этом происходящему в нераковых тканях. Такие клоны нередко содержат мутации, традиционно ассоциируемые с раковыми заболеваниями, однако их клинические последствия в нормальном организме могут быть разными и далеко не всегда патологическими.
Соматические мутации также тесно связаны с развитием широкого спектра заболеваний, помимо рака. Примером служат неврологические расстройства, вызванные постзиготными мутациями, влияющими на развитие и функцию мозга. Нарушения в пути PI3K–AKT–mTOR могут привести к мозговым мальформациям и эпилепсии. Кроме того, изменения в генах иммунной системы и регулирующих воспаление могут лежать в основе аутоиммунных заболеваний и сосудистых патологий. Некоторые мутации, появляющиеся на ранних этапах развития, вызывают хромосомные расстройства, приводящие к синдрому VEXAS и другим тяжелым патологиям.
Технологический аспект исследования соматической мозаичности крайне сложен из-за маленькой доли мутировавших клеток и высокой вероятности ошибок секвенирования. SMaHT применяет несколько параллельных подходов, включая тщательную работу с одиночными клетками, клонирование клеточных популяций для углубленного анализа и прямое отслеживание мутаций через анализ РНК. При этом используется инновационный методatuur дуплексного секвенирования, позволяющий с высокой точностью выявлять редкие вариации и исключать артефакты. Кроме обнаружения мутаций, исследователи SMaHT разрабатывают инструменты для оценки влияния этих генетических изменений на фенотип клеток. Совмещение данных о мутациях с анализом транскриптома, протеома, эпигенома и других омics-профилей позволяет выявить конкретные пути, на которые воздействуют соматические варианты.
Такая интеграция расширяет возможности понимания механизмов развития болезней и адаптации тканей. Еще один важный аспект работы сети — создание донор-специфических сборок генома с использованием методов длительного и ультра-длинного секвенирования. Это повышает точность выявления структурных вариантов в сложно аннотированных участках, таких как центромеры, теломеры и повторяющиеся области, а также позволяет более детально исследовать мутации, которые ранее были трудноуловимы. В биологическом плане картина, вырисовывающаяся благодаря SMaHT, показывает, что соматическая мозаичность — это не просто фон «ошибок», а динамичный процесс, тесно связанный с развитием, старением и функционированием организма. Она отражает баланс между накоплением повреждений, их ремонтом и отбором клеток, что в итоге формирует уникальное генетическое разнообразие каждого человека в масштабе отдельного органа и всего тела.
Настоящие и будущие исследования, объединенные в SMaHT, могут значительно изменить представления о роли генетической вариации внутри организма. Понимание механизмов формирования соматических мутаций и их клональных разрастаний способно открыть новые пути для разработки персонализированных методов диагностики и терапии целого спектра заболеваний, от нейродегенеративных состояний до рака. Главная миссия проекта — создать репрезентативный и широко доступный каталог соматических мутаций, который поможет исследователям всего мира писать новую главу в понимании человеческой биологии. Этот масштабный подход охватывает не только ядро генетики, но и этические, социальные и технологические вызовы современного биомедицинского исследования. SMaHT ведет активное сотрудничество с другими крупными геномными инициативами, такими как Human Pangenome Reference Consortium и PsychENCODE, что способствует интеграции данных, расширяет возможности анализа и способствует быстрому внедрению научных открытий в клиническую практику.
Таким образом, сеть Somatic Mosaicism across Human Tissues представляет собой революционную платформу, объединяющую новейшие технологии секвенирования, междисциплинарные команды ученых и богатый ресурс образцов, что позволяет глубоко и всесторонне исследовать феномен соматической мозаичности. Ее итоги обещают стать ключом к разгадкам механизмов старения, патогенеза многих заболеваний и поиску новых целевых точек для лечения, что несомненно изменит будущее медицины и геномных наук.