В современном мире остро стоят вопросы устойчивого использования ресурсов и экологической безопасности отходов жизнедеятельности человека. Моча, как жидкие отходы, традиционно воспринимается лишь как объект утилизации, требующий затрат энергии и средств на очистку. Однако последние достижения биотехнологии открывают новые перспективы для превращения мочи в полезные материалы с высокой добавленной стоимостью. Одним из таких инновационных решений стала разработка уникальной синтетической платформы Osteoyeast, способной превращать мочу непосредственно в гидроксиапатит — основной минеральный компонент костей и зубов, применяемый в медицине и промышленности. Гидроксиапатит (ГАП) — это биосовместимый материал, представляющий собой кальций-фосфатный минерал с формулой Ca5(PO4)3OH.
Благодаря своей структуре и химическим свойствам гидроксиапатит широко применяется в ортопедии, стоматологии, пластической хирургии, а также в производстве биоматериалов, фильтров для очистки воды и других промышленных изделий. Рынок ГАП стабильно растет, и к 2030 году его стоимость прогнозируется в несколько миллиардов долларов, что делает производство этого вещества крайне привлекательным с экономической точки зрения. Традиционные методы производства гидроксиапатита связаны с высокими энергетическими затратами и использованием сырья, иногда ограниченного природными ресурсами. В связи с этим идея создания устойчивого и рентабельного способа производства ГАП из отходов жизнедеятельности вызвала большой интерес ученых и предпринимателей. В этом контексте платформа Osteoyeast выступает как революционное решение, позволяющее использовать урею и другие питательные вещества из мочи для биосинтеза гидроксиапатита с помощью специально разработанной дрожжевой клетки.
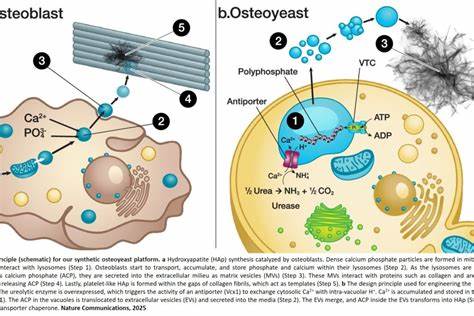
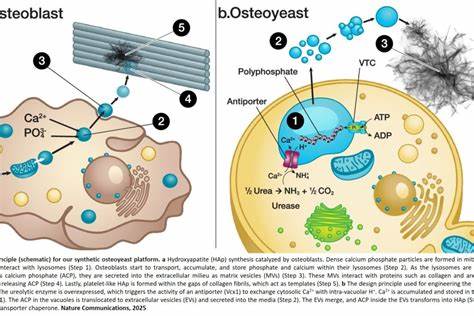
Основу платформы составляет дрожжевой штамм Saccharomyces boulardii, генетически модифицированный для повышения активности уреолизирующих ферментов. Эти ферменты способны разрушать мочевину, основной компонент мочи, что приводит к повышению pH вокруг клетки. Такой сдвиг кислотности активирует специализированный антипортёр Vcx1, который участвует в транспортировке и накоплении ионов кальция и фосфата во внутриклеточных вакуолях. Там формируется аморфный кальций-фосфат, который далее секретируется дрожжевой клеткой в виде внеклеточных везикул — миниатюрных мембранных пузырьков. В этих везикулах аморфное соединение постепенно кристаллизуется и превращается в гидроксиапатит.
Данные процессы напоминают естественный механизм минерализации костной ткани, где клетки-остеобласты синтезируют и выделяют кальциевый фосфат для формирования костного матрикса. Применение такого биологического принципа для инженерных дрожжевых клеток позволило ученым добиться продукции гидроксиапатита в концентрациях, превышающих 1 грамм на литр непосредственно из мочи, что является значительным достижением для биотехнологической индустрии. Уникальность технологии заключается также в том, что процесс происходит при умеренных температуре и pH, без необходимости использования сложного оборудования или дорогостоящих химикатов. Такой биопроцесс значительно снижает энергетические затраты и минимизирует экологический след по сравнению с традиционными методами. Кроме того, эффективность утилизации основного компонента мочи — урея, позволяет не только избавиться от потенциально опасных отходов, но и получить высококачественный продукт с высокой коммерческой ценностью.
Экономический анализ технологии показывает её высокую конкурентоспособность. Минимальная цена продажи гидроксиапатита, произведенного с помощью Osteoyeast, значительно ниже рыночных цен на сырьевые ГАП материалы разных сортов. Это, в сочетании с возможностью масштабирования производства в рамках городских или региональных систем утилизации отходов, открывает реальный путь к коммерчески успешному применению биотехнологии. Кроме финансовых аспектов, важным преимуществом является экологическая значимость. Текущие методы очистки сточных вод, включая мочу, требуют больших затрат воды, энергии и приводят к выбросам парниковых газов.
Многоступенчатая переработка мочи в биотехнологическом цикле с получением гидроксиапатита позволяет сократить количество питательных веществ, поступающих в водоемы и вызывающих эвтрофикацию — масштабную экологическую проблему, связанную с избыточным ростом водорослей и гибелью водных экосистем. Платформа Osteoyeast разрабатывалась на основе комплексного изучения биологии вакуолей дрожжей, которые являются аналогами лизосом — органелл, участвующих в хранении и регуляции ионов и биомолекул. В природных организмах липидные везикулы часто служат средой для транспортировки минералов. Использование подобного механизма в искусственно созданном штамме позволило добиться контролируемого синтеза и выделения аморфных кальций-фосфатных частиц, улучшающих выход и качество конечного гидроксиапатита. Чтобы подтвердить механизм и структуру получаемого материала, ученые применяли ряд современных методов исследования, включая трансмиссионную электронную микроскопию и рентгеновскую дифракцию.
Были идентифицированы кристаллические структуры ГАП, сопоставимые по свойствам с аналогами из костной ткани, что свидетельствует о высокой биосовместимости и практической применимости продукта. Флуоресцентные метки помогли проследить локализацию ионов кальция внутри клеток и в выделяемых везикулах, подтверждая последовательность биосинтетических событий. Биотехнологическая платформа также предлагает возможности для дальнейшей оптимизации. Увеличение продуктивности связано с улучшением транспортных процессов и секреции везикул, что потенциально может повысить выход гидроксиапатита и расширить его вариативность по размерам и морфологии. Эти свойства важны для адаптации материала под разные технические задачи — от имплантов в медицине до функциональных покрытий и очистных систем.
Кроме прямой пользы в производстве ценных биоматериалов, технология предоставила новый модельный объект для изучения процессов биоминерализации. Сложность и дороговизна исследований на клетках остеобластов или морских беспозвоночных часто ограничивают экспериментальные возможности. Использование генетически управляемого дрожжевого организма открывает перспективы для фундаментальных исследований механики и регуляции минерализации, а также разработки биоинженерных подходов к созданию новых материалов. Внедрение данной технологии в городскую инфраструктуру утилизации мочи может стать важным шагом к круговой экономике и снижению нагрузки на окружающую среду. Распределенные биореакторы с Osteoyeast способны обрабатывать поток мочи от десятков тысяч человек, сокращая необходимость централизованных очистных сооружений и снижая связанные с ними затраты.
Регулярный сбор и переработка выделенного гидроксиапатита позволит создавать новые экономические и социальные ценности на базе отходов, стимулируя устойчивое развитие городов. Перспективы развития платформы включают расширение спектра производимых материалов и интеграцию с другими биотехнологическими процессами для переработки органических отходов и восстановления ресурсов. Кроме того, можно ожидать появления новых применений гидроксиапатита, например, в экологически чистых конструкционных материалах, замене пластика, фильтрации воды и защите окружающей среды от тяжелых металлов и фтора. Таким образом, синтетическая платформа Osteoyeast представляет собой впечатляющее сочетание достижений молекулярной биологии, микробиологии и инженерии, направленное на решение актуальных глобальных задач. Производство гидроксиапатита из мочи с использованием генетически модифицированных дрожжей не только снижает экологический след и стимулирует экономические преимущества утилизации отходов, но и открывает новые горизонты в биоматериаловедении и устойчивой промышленности.
В условиях растущего спроса на экологичные материалы и ресурсоэффективные технологии, подобные инновации обещают существенный вклад в формирование биобезопасного и устойчивого будущего.




![Building art like an engineer [video]](/images/0DFB1CEB-FD7B-4849-9BDE-CCA58CF69F90)