История человеческих болезней насчитывает тысячи лет, но одними из самых важных прорывов в понимании их происхождения и эволюции стали исследования древней ДНК. Совсем недавно международная группа ученых сумела проследить генетическую историю более чем двухсот заболеваний, охватывающую период в 37 000 лет на территории Европы и Азии. Итоги этого масштабного исследования не только переосмысливают понимание антропогенного воздействия на распространение заболеваний, но и позволяют лучше понять, как именно связь человека с животными через тысячелетия изменила судьбу здоровья целых цивилизаций. Зоонозы, или заболевания, передающиеся от животных к человеку, известны человечеству давно. Сегодня к таким болезням относятся коронавирус, малярия, болезнь Лайма и многие другие, при этом они составляют значительную часть всех инфекционных заболеваний.
По оценкам, шесть из десяти известных инфекций и три из четырех новых или вновь возникающих заболеваний имеют природное животное происхождение. Способность патогенов переходить от животного к человеку, что называется «спилловером», становится центральным элементом в изучении эволюции болезней. Традиционно ученые предполагали, что распространение зоонозных инфекций было тесно связано с одомашниванием животных в древние времена. Однако, до недавнего времени не было убедительных генетических данных, подкрепляющих конкретные временные рамки и причины этого явления. Новое исследование предоставляет убедительные доказательства того, что всплеск зоонозных заболеваний произошел примерно 6 500 лет назад, с пиком распространения около 5 000 лет назад.
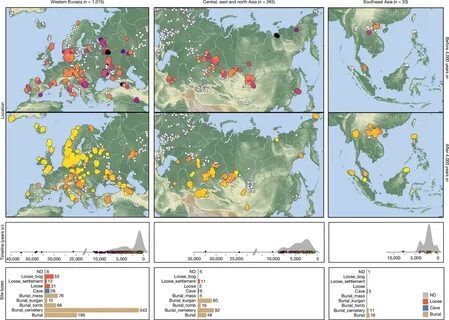
Удивительно, что эти даты несколько позже периодов одомашнивания скота в Месопотамии и Юго-Восточной Азии, что ставит под сомнение прежние гипотезы и заставляет исследователей взглянуть на процесс эволюции болезней с иной перспективы. В ходе исследования ученые проанализировали микробную ДНК из зубов и костей 1 313 древних человеческих останков, найденных на территории Евразии. Было выявлено 5 486 последовательностей ДНК бактерий, паразитов и вирусов, что позволило впервые на таком масштабе реконструировать историю инфекционных заболеваний. Результаты показали, что первые очаги зоонозов возникли в основном в Азии и России, совпадая с изменением образа жизни людей – от охоты и собирательства к скотоводству и земледелию. Одним из ключевых факторов ускорения распространения болезней стало кочевое скотоводство.
Обученные лошади и повозки, запряжённые волами, позволяли кочевникам совершать дальние путешествия, торговать и контактировать с другими группами, тем самым способствуя миграции патогенов. Такой образ жизни не только увеличивал риск заражения новыми заразными агентами, но и стимулировал адаптацию иммунной системы человека к меняющимся условиям. Особый интерес вызывает вывод о том, что мутации в зоонозных патогенах способствовали укреплению иммунитета у кочевых народов, однако у оседлых земледельцев и охотников-собирателей иммунные реакции были менее эффективны, что делало их более уязвимыми к новым заболеваниям. В то же время, сильная иммунизация могла привести к появлению хронических болезней, таких как рассеянный склероз, что подтверждается недавними генетическими исследованиями. Это демонстрирует сложную двустороннюю динамику взаимодействия между патогенами и человеческим организмом, развивавшуюся тысячелетиями.
В исследовании были обнаружены древнейшие генетические следы возбудителей многих известных инфекций. Например, в образце возрастом около 5 500 лет были идентифицированы ДНК Yersinia pestis – бактерии, ответственной за черную смерть, которая в Средние века унесла жизни миллионов в Европе. Это служит напоминанием о том, насколько зоонозы влияли не только на здоровье, но и на социально-исторические процессы, включая миграции, демографические катастрофы и эволюционные адаптации. Кроме того, выявлены следы таких болезней, как малярия (возраст около 4 200 лет), лепра (около 1 400 лет), гепатит В (примерно 9 800 лет) и дифтерия (около 11 100 лет). Эти данные позволяют проследить влияние инфекций на человеческие общества с далекого прошлого до недавних времен.
Несмотря на революционные открытия, исследователи отмечают определённые ограничения работы. В частности, вирусные гены на основе РНК не были проанализированы, что могло привести к упущению некоторых патогенов. Кроме того, исследуемые останки сосредоточены в основном на Евразии, а данные из Африки и других регионов остаются недостаточно изученными из-за ограниченного доступа к древнему ДНК материалу. Понимание исторического развития инфекционных болезней крайне важно не только с академической точки зрения, но и для создания эффективных современных профилактических и лечебных стратегий. Эволюционные мутации патогенов, изученные в древних образцах, помогают прогнозировать возможные изменения в структурах вирусов и бактерий, что необходимо учитывать при разработке новых вакцин и лекарств.
Знания о прошлом дают нам ключ к будущему, помогая быть готовыми к новым вызовам в области здоровья и безопасности населения. Этот масштабный проект, возглавленный Эской Виллерслевом и Мартином Сикорой, показывает, как междисциплинарный подход с использованием генетики, археологии и истории может раскрыть глубокие взаимосвязи между культурными изменениями и эволюцией заболеваний. Благодаря современным методам секвенирования древней ДНК мы теперь обладаем уникальной возможностью взглянуть на то, как тысячи лет назад начало происходить одно из важнейших явлений в истории человечества – рост и распространение зоонозов. Эксперты уверены, что дальнейшее расширение подобных исследований с включением широкой географии и анализа РНК-вирусов позволит еще более полно понять динамику возникновения и эволюции инфекционных заболеваний. Это не только поможет лучше разобраться в исторических эпидемиях, но и повысит готовность человечества к будущим вспышкам болезней, которые могут возникать по тем же природным механизмам.
Таким образом, изучение 37 000 лет истории болезней Европы и Азии открывает новую главу в понимании того, каким образом миграции, изменения образа жизни и взаимодействие человека с животным миром сформировали не только нашу культуру и общество, но и биологическую устойчивость к инфекциям. Этот масштабный научный труд является важным шагом на пути к предотвращению распространения опасных заболеваний и обеспечению здоровья будущих поколений.