Старение - это естественный процесс, сопровождающийся постепенным снижением функциональной активности тканей и органов. На клеточном уровне оно характеризуется накоплением повреждений, уменьшением численности и активности стволовых клеток, а также развитием хронического воспаления. Одной из главных причин возрастных изменений считается сенесценция клеток - состояние, когда клетки теряют способность к делению и начинают выделять провоспалительные факторы, усугубляя деградацию тканей. По мере накопления таких клеток их воздействие становится все более заметным, что способствует развитию возрастных заболеваний и снижает качество жизни. Однако современные биомедицинские исследования открывают новые горизонты для борьбы с этим процессом.
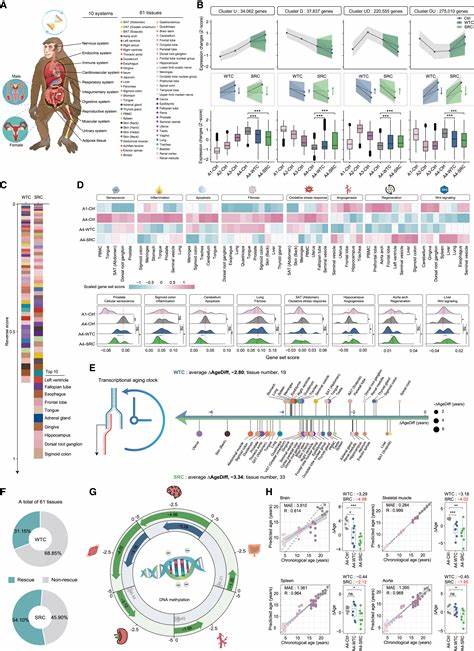
Одной из самых перспективных стратегий является использование генетически модифицированных сенесценция-устойчивых клеток для восполнения и омоложения тканей. Недавние исследования, проведённые на приматах, демонстрируют впечатляющие результаты в этой области. В частности, учёные создали специальный тип человеческих мезенхимальных прогениторных клеток, усиленных с помощью генной инженерии, чтобы сделать их устойчивыми к развитию сенесценции. Эти клетки получили обозначение SRCs (senescence-resistant cells) и были протестированы на старых макаках в ходе протяжённого эксперимента продолжительностью 44 недели. Результаты применения SRCs превзошли ожидания: наблюдалось системное снижение маркеров старения, уменьшение хронического воспаления и признаки восстановления тканей без каких-либо побочных эффектов.
Данные свидетельствуют о том, что введённые SRCs не только восстанавливали ткани, но и оказывали положительное влияние на головной мозг - улучшалось строение его архитектуры, повышались когнитивные способности животных. Также удивительным оказалось влияние на репродуктивную систему: благодаря лечению прошло замедление возрастных изменений и некоторого регенерационного восстановления. Важную роль в терапевтическом эффекте SRCs сыграли выделяемые ими экзосомы - мельчайшие везикулы, содержащие биологически активные молекулы. Экзосомы способны переносить полезные вещества и сигнальные молекулы к клеткам и тканям, способствуя снижению сенесценции и активируя процессы регенерации. Таким образом, эффективность SRCs базируется не только на их способности замещать устаревшие клетки, но и на их роли в межклеточной коммуникации, обеспечивая комплексное омоложение организма.
Главным преимуществом SRCs является их генетическая модификация, нацеленная на повышение устойчивости к стрессам и механизмам клеточного старения. Ключевым элементом в этом процессе стал ген FOXO3, известный своим влиянием на продление жизни и регуляцию клеточных защитных систем. Именно через усиление активности FOXO3 удалось достичь стойкой сопротивляемости сенесценции и улучшить восстановительные функции клеток. Этот подход становится важным шагом вперёд на пути от борьбы с симптомами старения к целенаправленной регенеративной терапии, способной замедлять и даже частично обратимо изменять возрастные процессы. Применение таких клеток у приматов является важным этапом перед переходом на людские клинические испытания.
Существует многообещающий потенциал в лечении возрастных заболеваний, дегенеративных состояний мозга, а также в поддержке репродуктивного здоровья и общего метаболического баланса. Наряду с этим, особое внимание уделяется безопасности и долговременной эффективности. В ходе проведённого исследования не выявлено серьёзных побочных эффектов, что вселяет оптимизм в возможность использования SRCs на практике. Кроме того, подобные разработки вписываются в общую тенденцию современной медицины - переход к персонализированным регенеративным технологиям с применением клеточных и генетических методов. Исследования все чаще подтверждают, что именно клеточный потенциал и возможности перепрограммирования существенно влияют на скорость и качество старения.
Ранее масштабное внимание уделялось фармакологическим способам замедления старения, таким как сенолитики - препараты, способные избирательно уничтожать сенесцентные клетки. Однако такие методы обладают ограничениям, и их долгосрочные эффекты еще изучаются. В свою очередь, использование устойчивых к старению мезенхимальных клеток представляет собой гораздо более естественный способ восстановления тканей и поддержания гомеостаза. Терапия SRCs не ограничивается одним органом или системой, а оказывает системное воздействие, что благоприятно сказывается на состоянии всего организма. Одним из ключевых открытий стало то, что SRCs способны улучшать функции мозга, что подтверждается улучшением когнитивных показателей у исследуемых приматов.
Возрастное снижение когнитивных способностей связывается не только с потерей нейронов, но и с ухудшением кровоснабжения, повышением воспалительных процессов и дисбалансом в микросредах мозга. SRCs, благодаря своему потенциалу противодействовать этим факторам, способствуют восстановлению нейрональных сетей и повышают умственную активность. Воздействие на репродуктивную систему также особенно актуально, так как с возрастом у самцов и самок приматов наблюдается снижение гормонального фона, ухудшение качества гамет и сниженная фертильность. SRCs способны замедлить эти процессы, обеспечивая обновление клеток и улучшение микроокружения репродуктивных органов. Современные методы генетического редактирования, использованные для создания SRCs, включают передовые технологии, обеспечивающие безопасность и точность внесённых изменений.
Они позволяют минимизировать риск мутаций и нежелательных эффектов, что особенно важно для клинического применения. Вдобавок к этому, экзосомы SRCs могут применяться как самостоятельное клеточное средство, что открывает перспективы для менее инвазивных методов регенеративной медицины. По мере углубления исследований и проведения дальнейших клинических испытаний возможно появление полностью новых терапевтических подходов к борьбе со старением и связанными с ним заболеваниями. В целом изучение и применение сенесценция-устойчивых клеток у приматов представляет собой прорыв в современной биомедицине. Эта технология способна не только продлить биологическую молодость органов и систем, но и существенно улучшить качество жизни в старшем возрасте.
В контексте растущего интереса общества к долголетию и здоровому старению такие открытия получают высокую значимость и создают фундамент для будущих медицинских достижений. Такая интеграция клеточных и генетических методов, поддержанная комплексным анализом эффектов и длительным наблюдением, направлена на гарантированное улучшение здоровья и функциональности организма без компромиссов по безопасности. Итогом считается открытие перспективных возможностей для разработки новых регенеративных лекарственных средств, которые смогут адресно воздействовать на механизмы старения, изменяя их в пользу поддержания молодости. Ранее многие попытки высокотехнологичного вмешательства в процессы старения были ограничены сложности доставки или отсутствием устойчивости новых клеток. Сейчас создание SRCs позволяет считать эти проблемы преодолёнными, что делает данную методику одним из наиболее перспективных направлений биомедицины XXI века.
Очевидно, что дальнейшее развитие и адаптация технологии к человеческим клиническим условиям станет новым этапом в борьбе с возрастной дегенерацией, улучшая перспективы миллионов людей по всему миру. Таким образом, используется синергия достижений в стволовой терапии, генной инженерии и молекулярной биологии для комплексного решения возрастных проблем, ранее считавшихся неизбежными и не поддающимися изменению. .